PROTECCIÓN CONTRA LA CORROSIÓN
Todo metal puede ser dañado por la corrosión, sólo por el hecho de estar expuesto al medio que lo rodea se origina una reacción fisicoquímica que puede debilitar el material o puede llegar al punto de destruirlo, se estima que el promedio de vida útil de un metal que no está protegido contra está es de dos años, un tiempo de vida corto a la hora de hablar de utilidades y más si este puede ser prevenido.
Luego de haber analizado la corrosión y sus formas, se presentaran algunos métodos que se tienen hoy en día para prevenirla, como los son recubrimientos metálicos, inorgánicos y orgánicos, que se aplican a los metales para prevenir o reducir la corrosión.
RECUBRIMIENTOS METÁLICOS
Uno de los procedimientos más empleados contra la oxidación y corrosión es el recubrir la superficie que se desea proteger con una capa de metal auto protector lo más compacta y adherente posible.
Si el metal protegido es menos electronegativo (catódico) que el protector (anódico), la protección tiene lugar aun en el caso de agrietamiento o descascarillado de la capa protectora, como ejemplo de este caso tenemos el acero recubierto de Zn. Lo contrario sucede si el recubrimiento es catódico, requiriéndose en este caso un recubrimiento perfecto, sin porosidad, para este caso tenemos acero al recubierto de Sn. La elección del metal empleado en el recubrimiento se hace de acuerdo con el metal que se ha de proteger, del objeto de que se trata y del espesor que se proyecta dar a la capa protectora. Los recubrimientos metálicos pueden aplicarse por varios procedimientos: por electrólisis, por inmersión en el baño del metal protector, por metalización, por cementación y por chapado.
Preparación de la superficie: Cualquiera que sea el recubrimiento que se adopte, debe desengrasarse previamente la pieza con un disolvente apropiado, como, tricloroetileno, sosa cáustica, benceno, etc. Después se elimina el orín y cascarilla de la superficie del metal sometiéndolo a un decapado que consiste en la eliminación de la capa de laminación y del orín en la superficie de las piezas de acero, es absolutamente necesaria antes de aplicar un recubrimiento de cualquier clase y puede efectuarse por procedimientos mecánicos, químicos y electrolíticos. [1]
En este capítulo se trataran los recubrimientos metálicos, estos se obtienen por diversos procedimientos, el principio de protección frente a la corrosión es diferente según la naturaleza del metal de recubrimiento, en este artículo sólo nos enfocaremos en dos tipos de procesos: recubrimiento metálico por inmersión y recubrimiento metálico por electro deposición [2]
ELECTRODEPOSICIÓN
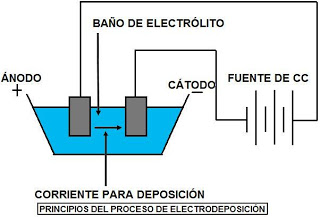
La electrodeposición es un procedimiento electroquímico mediante el cual se logra cubrir una pieza con una fina capa de determinado metal. Para lograrlo se sumerge la pieza a cubrir en una solución electrolítica que contiene los iones del metal que formará la capa.
La pieza se pondrá en contacto con una fuente de corriente continua y con un electrodo que cumplirá la función de ánodo, cediendo electrones para que los iones metálicos en solución se reduzcan y se depositen sobre la pieza, que cumple la función de cátodo. De esta manera se obtiene el recubrimiento metálico en la pieza.
[3] En la anterior figura se muestra el proceso de electrodeposición
Recordemos que el ánodo de este sistema estará hecho del metal con que se quiere recubrir la pieza, para que pueda disolverse, oxidarse, cediendo electrones y aportando iones a la solución, a medida que los iones que estaban presentes en la solución, se reducen y se depositan sobre la pieza a recubrir, que funciona como cátodo en el sistema. Todo este proceso es posible gracias a la corriente continua que permite la movilización de electrones.
Otro punto a destacar es que las propiedades que tendrá la capa que recubre la pieza, depende directamente de la corriente que se haya aplicado. La adherencia de la capa, su calidad, la velocidad de deposición, dependen del voltaje y de otros factores relacionados con la corriente aplicada.
También hay que tener en cuenta que si el objeto a recubrir tiene una superficie intrincada, la capa formada será más gruesa en algunos puntos y más fina en otros. De todos modos, existen maneras de eludir este inconveniente, por ejemplo, utilizando un ánodo con forma similar a la de la pieza a recubrir.
Este procedimiento es utilizado para brindarle resistencia a la corrosión a una determinada pieza, también para que aumente su resistencia a la abrasión, para mejorar su estética, entre otras funciones.[4]
CROMADO POR INMERSIÓN
El cromo es un material muy resistente a la oxidación y la corrosión por los que sus propiedades son muy útiles en este tipo de procesos pero su metalurgia es muy difícil por lo cual la única o la mejor forma de hacer un recubrimiento metálico con este material es por electrolisis, este proceso ayuda a proteger el material contra la corrosión y además de esto ayuda a mejorar su aspecto.
En la mayoría de casos la capa de cromo que queda no es totalmente uniforme, en el proceso por lo general queda un espesor mayor al necesario por lo que las piezas deben ser rectificadas para conseguir los acabados adecuados. El cromo se aplica bien sobre el cobre, el níquel y el acero pero no sobre el zinc o algún tipo de fundición.
Antes de comenzar el proceso de cromado deberemos alistar la superficie con otros procesos para que el cromado pueda tener el resultado correcto, dichos procesos son:
- Proceso de decapado: consiste en la eliminación de impurezas en la superficie del material tales como manchas, herrumbres o escoria, esto se lleva acabo utilizando ácidos que reaccionan con la superficie eliminando así sus impurezas. Los ácidos más usados para este proceso son ácido sulfúrico y ácido clorhídrico.
- Pulido: se dice que es necesario un pulido antes del cromado para una mejor adherencia del cromo a la superficie pero también se ha apreciado con el paso del tiempo que el cromado sobre una superficie anteriormente pulida tiende a ser más resistente contra la corrosión y la abrasión, sin contar con que la pieza queda con un mejor acabado, es más utilizado comúnmente cuando se quiere dar un acabado muy brillante o decorativo.
- Desengrases previos: esto es un proceso vital en todo material dispuesto a recibir un depósito electrolítico y de la eficacia de este depende la adherencia del depósito metálico, este se puede hacer de distintas formas entre las cuales están: manualmente mediante el cepillado con cal de Viena, cepillando la pieza con un cepillo de bronce y cepillando la pieza previamente mojada con una solución jabonosa.
- Cobreado: este proceso es importante y muy útil a la hora de cromar piezas de hierro ya que el cromo tiene una mejor adherencia sobre superficies de cobre o níquel, y su aplicación se hace a través de un proceso de electrolisis.
Por ultimo deberemos aplicar un baño de níquel para garantizar la mayor eficacia del proceso de cromado.[5]
Después de haber pasado el material por todos estos procesos, está listo para ser cromado. En esta práctica se aplica una muy delgada capa de cromo sobre un metal o material base para que este se encuentre protegido de la corrosión, el cromado se efectúa mediante una solución de ácido crómico, que contiene una pequeña proporción de ácido sulfúrico a la cual se le agrega un poco de sulfato sódico. La relación de ácido crómico a sulfato lo mejor es mantener esta en 100:1 y no salirse de los límites 200:1 o 50:1.
En el proceso electrolítico, la corriente puede ser suministrada por una batería de 6V con el polo negativo conectado al objeto y el lado positivo al ánodo, el buen resultado del cromado depende de varios parámetros como, mantener la relación de ácido crómico a sulfato, conservar la temperatura del baño a una temperatura constante de unos 35°C y mantener la corriente a una razón de 75A por cada decímetro cuadrado de superficie a cromar.
Fracciones de corrientes usadas para cromar objetos pequeños.
1cm2 __0.0833A 5cm2___0.4165A 10cm2___0.833A
El poder de penetración del cromado es muy bajo pero hay formas de aumentar un poco esto, para determinadas temperaturas aumentar el flujo de corriente ayudar a elevar el poder de penetración, también se ha descubierto que las soluciones de cromado con baja densidad tienen mayor poder de penetración.[6]
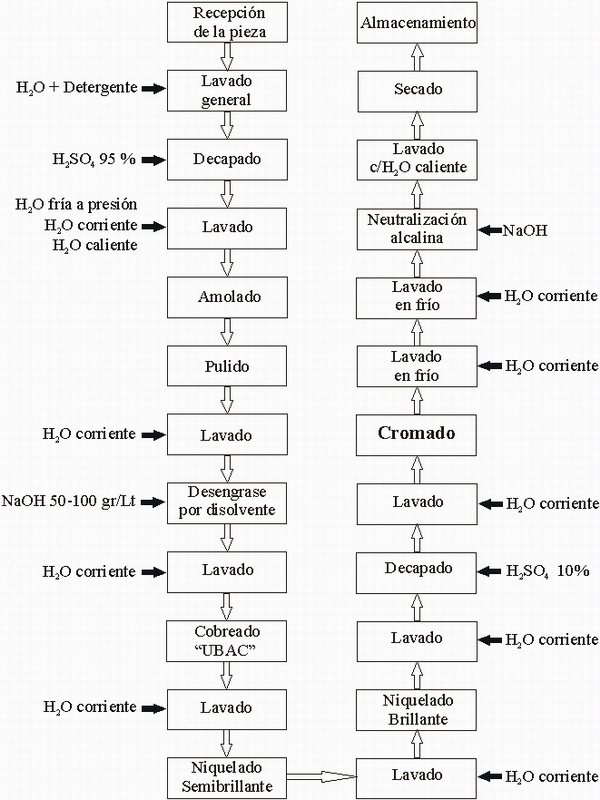
DIAGRAMA DE FLUJO DEL PROCESO
[7] En la imagen anterior se presenta el diagrama de flujo de proceso de cromado
PRODUCTO FINAL DEL PROCESO DE CROMADO
DEFECTOS DEL CROMADO
Entre los defectos más comunes del cromado están:
- Depósitos estriados: se pueden apreciar rayas blancas sobre la superficie y pueden ser causados por usas densidades de corriente muy bajas en el proceso.
- Depósitos de color mate: estos pueden ser causados por las bajas temperaturas a las que se realiza el cromado.
- Depósitos quemados: son causados por una densidad de corriente excesiva [8]
GALVANIZADO POR INMERSIÓN
Consiste en cubrir una porción de metal (acero), con una capa delgada de zinc. Este elemento debe estar perfectamente limpio para eso el metal se sumerge en un recipiente con ácido sulfúrico diluido quitando todas las imperfecciones que la pieza pueda tener, a este proceso se le conoce como decapado. Este se puede realizar por medio de un galvanizado por inmersión en caliente o un galvanizado por inmersión en continuo.
El galvanizado por inmersión en caliente se logra a una temperatura de 450 grados Celsius y consiste en alear el zinc con el acero.
El galvanizado en continuo es utilizado para acero laminado de medio, bajo y alto carbono donde se limpian bien las piezas de calientan y luego se les agrega una capa de zinc para obtener una aleación zinc acero.
Este proceso se realiza con el fin de proteger las piezas de metal contra la corrosión debido a que las condiciones atmosféricas como el contacto continuo con el agua y el sol produce en los materiales un deterioro muy rápido.[9]
ESTAÑO POR INMERSIÓN
Los elementos metálicos son recubiertos por una máquina de estañado que consta de un recipiente controlado termostáticamente que contiene el estaño, luego la pieza pasa a través de dos rodillos que controlan el espesor de la capa de estaño para esto el metal se debe haber sometido a un proceso de limpieza llamada decapado.
Los elementos más comunes que son sometido a estañado son los envases de alimentos debido a que el estaño tiene propiedades no toxicas, son muy resistentes a la corrosión siempre y cuando no halla ruptura del estaño, y son muy fáciles de soldar.
[10]En la imagen anterior se muestra un pilar de acero recubierto con 0.2 micras de estaño
BIBLIOGRAFIA
[1] Autor FRANCISCO LUIS CUESTA FERNANDEZ
http://www.eduinnova.es/monografias09/Nov09/Corrosion.pdf
[2] http://www.upv.es/materiales/Fcm/Fcm12/pfcm12_5_6.html
[3] http://electromaquinado.blogspot.com.co/2009/07/maquinado-electroquimico.html
[4] http://quimica.laguia2000.com/conceptos-basicos/electrodeposicion#ixzz3tpjHcUGE
[5] http://tecnicadelcromado.blogspot.com.co/
[6] http://www.monografias.com/trabajos33/cromado-electrolitico/cromado-electrolitico2.shtml
[10] http://app.idu.gov.co/geodata/doc/guia_galvanizado_24nov14%20(1).pdf
Jefferson Bayer bedoya 1088332645
Valentina Camacho 1088336080
Daniela Rodas Rodriguez 1088336530
Luis Alberto Vargas 1088325609